Alessio Nencioni, Irene Caffa, Salvatore Cortellino
Tóm tắt | Sự tổn thương của các tế bào ung thư đối với sự thiếu hụt chất dinh dưỡng và sự phụ thuộc của chúng vào các chất chuyển hóa cụ thể là dấu hiệu nổi bật của bệnh ung thư. Chế độ ăn kiêng nhịn ăn hoặc nhịn ăn (FMDs) dẫn đến sự thay đổi lớn về các yếu tố tăng trưởng và mức độ chuyển hóa, tạo ra môi trường có thể làm giảm khả năng của các tế bào ung thư để thích nghi và tồn tại và do đó cải thiện hiệu quả của các liệu pháp điều trị ung thư. Ngoài ra, nhịn ăn hoặc FMD làm tăng khả năng kháng hóa trị trong các tế bào ung thư bình thường nhưng không thúc đẩy tái tạo ở các mô bình thường, điều này có thể giúp ngăn ngừa các tác dụng phụ có hại và có thể đe dọa đến tính mạng của phương pháp điều trị. Mặc dù bệnh nhân nhịn ăn hầu như không được bệnh nhân chấp nhận, cả nghiên cứu trên động vật và lâm sàng đều cho thấy các chu kỳ FMD có hàm lượng calo thấp là khả thi và an toàn chung. Một số thử nghiệm lâm sàng đánh giá hiệu quả của việc nhịn ăn hoặc FMD đối với các tác dụng phụ điều trị xuất hiện và kết quả hiệu quả đang diễn ra. Chúng tôi đề xuất rằng việc kết hợp FMD với hóa trị liệu, liệu pháp miễn dịch hoặc các phương pháp điều trị khác là một chiến lược đầy hứa hẹn để tăng hiệu quả điều trị, ngăn ngừa tình trạng kháng thuốc và giảm tác dụng phụ.
Các yếu tố liên quan đến chế độ ăn uống và lối sống là những yếu tố chính quyết định nguy cơ phát triển ung thư, với một số bệnh ung thư phụ thuộc vào thói quen ăn uống nhiều hơn những bệnh khác
Mặc dù trong thập kỷ qua, chúng ta đã chứng kiến những thay đổi chưa từng có và những tiến bộ đáng chú ý trong điều trị ung thư14,15, vẫn còn một nhu cầu quan trọng để có hiệu quả hơn và, có thể,
Nhịn ăn buộc các tế bào khỏe mạnh phải vào một phân chia chậm và chế độ được bảo vệ cao để bảo vệ chúng chống lại sự lăng mạ độc hại có nguồn gốc từ thuốc chống ung thư trong khi nhạy cảm với các loại tế bào ung thư khác nhau đối với các phương pháp trị liệu11,12,17 này. Khám phá này ngụ ý rằng một can thiệp chế độ ăn uống duy nhất có khả năng giúp giải quyết các khía cạnh khác nhau và không kém phần quan trọng của liệu pháp ung thư.
Trong bài viết Ý kiến này, chúng tôi thảo luận về cơ sở sinh học cho việc sử dụng chế độ ăn kiêng nhịn ăn hoặc nhịn ăn (FMDs) để làm giảm TEAEs mà còn để ngăn ngừa và điều trị ung thư. Chúng tôi cũng minh họa sự cẩn thận của phương pháp thử nghiệm này18,19 và các nghiên cứu lâm sàng được công bố và đang diễn ra trong đó nhịn ăn hoặc FMD đã được áp dụng cho bệnh nhân ung thư.
Nội dung
Phản ứng nhịn ăn theo hệ thống & tế bào
Nhịn ăn dẫn đến thay đổi hoạt động của nhiều con đường trao đổi chất liên quan đến việc chuyển sang chế độ có thể tạo ra năng lượng và các chất chuyển hóa bằng cách sử dụng các nguồn carbon được giải phóng chủ yếu từ mô mỡ và một phần từ cơ bắp. Những thay đổi về mức độ của các hoocmon và chất chuyển hóa lưu hành sẽ làm giảm sự phân chia tế bào và hoạt động trao đổi chất của các tế bào bình thường và cuối cùng bảo vệ chúng khỏi sự lăng mạ hóa trị liệu 11,12. Các tế bào ung thư, bằng cách không tuân theo các lệnh chống tăng trưởng được quy định bởi các điều kiện đói này, có thể có phản ứng ngược lại của các tế bào bình thường và do đó trở nên nhạy cảm với hóa trị liệu và các phương pháp điều trị ung thư khác.
Phản ứng có hệ thống đối với việc nhịn ăn
Phản ứng với việc nhịn ăn được phối hợp một phần bởi mức độ lưu thông của glucose, insulin, glucagon, hormone tăng trưởng (GH), IGF1, glucocorticoids
Glucagon và lượng insulin thấp cũng kích thích sự phân hủy chất béo trung tính (phần lớn được lưu trữ trong mô mỡ) thành glycerol và axit béo tự do. Trong thời gian nhịn ăn, hầu hết các mô sử dụng axit béo để làm năng lượng, trong khi não dựa vào glucose và dựa vào thể xeton do tế bào gan sản xuất (thể xeton có thể được tạo ra từ acetyl-CoA được tạo ra từ axit béo-oxy hóa hoặc từ axit amin xeton). Trong giai đoạn ketogenic của nhịn ăn, các thể xeton đạt đến nồng độ trong khoảng milimolar, thường bắt đầu sau 2-3 ngày kể từ khi bắt đầu nhịn ăn. Cùng với glycerol và axit amin có nguồn gốc từ chất béo, các thể xeton cung cấp năng lượng cho quá trình tạo gluconeogenesis, giúp duy trì lượng đường ở nồng độ xấp xỉ 4mM (70mg mỗi dl), phần lớn được não sử dụng.
Glucocorticoids và adrenaline cũng góp phần định hướng sự thích nghi trao đổi chất
Cuối cùng, nhịn ăn làm giảm mức độ lưu thông leptin, một loại hormone chủ yếu được tạo ra bởi các tế bào mỡ giúp ức chế cơn đói, đồng thời làm tăng mức độ adiponectin, làm tăng sự phân hủy axit béo23,24. Do đó, kết luận, đặc điểm nổi bật của phản ứng toàn thân của động vật có vú đối với việc nhịn ăn là nồng độ glucose và insulin thấp, nồng độ glucagon và ketone cao, hàm lượng IGF1 và leptin thấp và mức adiponectin cao.
Phản ứng tế bào để nhịn ăn
Phản ứng của các tế bào khỏe mạnh với việc nhịn ăn được bảo tồn về mặt tiến hóa và mang lại khả năng bảo vệ tế bào, và ít nhất là ở các sinh vật mô hình, đã được chứng minh là làm tăng tuổi thọ và sức khỏe. IGF12,22,25
Nhịn ăn và kết quả là hạn chế glucose sẽ ức chế hoạt động của PKA, tăng hoạt động AMPK và kích hoạt EGR1 và do đó đạt được tác dụng bảo vệ tế bào, bao gồm cả những tác dụng trong cơ tim 22,25,26. Cuối cùng, nhịn ăn và FMDs (xem bên dưới để biết thành phần của chúng) cũng có khả năng thúc đẩy các hiệu ứng tái tạo (Hộp 1) theo cơ chế phân tử, một số trong số đó có liên quan đến ung thư, chẳng hạn như tăng tự động hoặc cảm ứng hoạt động sirtuin22,37 49 .

Phương pháp ăn kiêng trong bệnh LMLM
Các phương pháp tiếp cận chế độ ăn uống dựa trên nhịn ăn đã được nghiên cứu rộng rãi hơn trong ung thư học, cả về mặt chính xác và lâm sàng, bao gồm nhịn ăn nước (kiêng tất cả thức ăn và đồ uống trừ nước) và FMDs 11,12,17,25,26,50 60 (Bảng 1). Dữ liệu lâm sàng sơ bộ chỉ ra rằng có thể cần nhanh ít nhất 48 giờ để đạt được các tác dụng có ý nghĩa lâm sàng trong ung thư học, chẳng hạn như ngăn ngừa tổn thương DNA do hóa trị gây ra đối với các mô khỏe mạnh và giúp duy trì
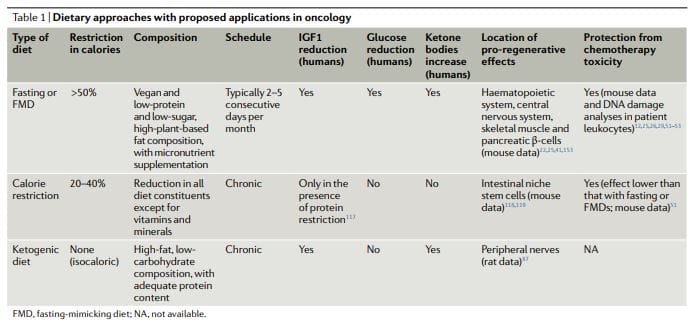
Tuy nhiên, hầu hết bệnh nhân đều từ chối hoặc gặp khó khăn khi hoàn thành chế độ nhịn ăn bằng nước, và khó có thể biện minh cho những nguy cơ tiềm ẩn của việc thiếu hụt calo và vi chất dinh dưỡng kéo dài liên quan đến nó. LMLM là chế độ ăn kiêng được thiết kế về mặt y tế rất ít calo (thường là từ 300 đến 1,100kcal mỗi ngày), đường và protein tái tạo nhiều tác dụng của việc nhịn ăn chỉ uống nước nhưng bệnh nhân tuân thủ tốt hơn và giảm nguy cơ dinh dưỡng22,61,62, 3. Trong thời gian bị LMLM, bệnh nhân thường được uống một lượng nước không hạn chế, các phần nhỏ, tiêu chuẩn hóa của nước canh rau, súp, nước trái cây, thanh hạt và trà thảo mộc, cũng như các chất bổ sung vi chất dinh dưỡng. Trong một nghiên cứu lâm sàng về 5 chu kỳ hàng tháng của bệnh LMLM kéo dài 1 ngày ở những người khỏe mạnh nói chung, chế độ ăn uống được dung nạp tốt và giảm lượng mỡ trong cơ thể và tổng lượng mỡ, huyết áp và mức IGF62. Trong các thử nghiệm lâm sàng ung thư trước đây và đang diễn ra, bệnh LMLM hoặc nhịn ăn thường được thực hiện sau mỗi 3 4 tuần, ví dụ, kết hợp với các phác đồ hóa trị, và thời gian của chúng dao động trong khoảng từ 1 đến 5 ngày52,53,58,61,63 68 . Điều quan trọng là, không có tác dụng phụ nghiêm trọng nào (cấp độ G3 trở lên, theo Tiêu chí thuật ngữ chung cho các sự kiện có hại) được báo cáo trong nghiên cứu này52,53,58,61.
Ketogenic Chế độ ăn uống
Chế độ ăn ketogenic (KD) là chế độ ăn kiêng có hàm lượng calo bình thường, hàm lượng chất béo cao và ít carbohydrate 69,70. Trong KD cổ điển, tỷ lệ giữa trọng lượng của chất béo và trọng lượng kết hợp của carbohydrate và protein là 4: 1. Cần lưu ý, FMDs cũng là ketogenic vì chúng có hàm lượng chất béo cao và có khả năng gây ra sự gia tăng đáng kể (0.5mmol mỗi lít) trong mức độ của các cơ thể ketone tuần hoàn. Ở người, KD cũng có thể làm giảm mức IGF1 và insulin (hơn 20% so với giá trị ban đầu), mặc dù những tác động này bị ảnh hưởng bởi mức độ và loại carbohydrate và protein trong chế độ ăn uống71. KD có thể làm giảm lượng đường trong máu, nhưng chúng thường duy trì trong giới hạn bình thường (nghĩa là> 4.4mmol mỗi lít) 71.
Đáng chú ý, KDs có thể có hiệu quả để ngăn chặn sự gia tăng glucose và insulin thường xảy ra để đáp ứng với các chất ức chế PI3K, vốn đã được đề xuất để hạn chế hiệu quả của chúng72. Theo truyền thống, KDs được sử dụng để điều trị chứng động kinh khó chữa, chủ yếu ở trẻ em69. Trong các mô hình chuột, KDs gây ra tác dụng chống ung thư, đặc biệt là ở u nguyên bào đệm 70,72. Các nghiên cứu lâm sàng chỉ ra rằng KDs có thể không có hoạt tính điều trị đáng kể khi được sử dụng như một tác nhân đơn lẻ ở bệnh nhân ung thư và gợi ý rằng nên tìm kiếm lợi ích tiềm năng của các chế độ ăn này kết hợp với các phương pháp tiếp cận khác, chẳng hạn như hóa trị, xạ trị, điều trị kháng nguyên, thuốc ức chế PI86K
KDs được báo cáo là có tác dụng bảo vệ thần kinh ở các dây thần kinh ngoại vi và ở vùng hải mã .87,88. Tuy nhiên, vẫn còn phải xác định liệu KDs cũng có tác dụng tăng sinh tương tự như nhịn ăn hoặc FMD (Hộp 1) và liệu KDs cũng có thể được sử dụng để bảo vệ động vật có vú còn sống khỏi độc tính của hóa trị. Đáng chú ý, tác dụng tái tạo của nhịn ăn hoặc FMD dường như được tối đa hóa bằng cách chuyển đổi từ chế độ phản ứng đói-đói, liên quan đến sự phân hủy các thành phần tế bào và cái chết của nhiều tế bào, và giai đoạn tái nuôi dưỡng, trong đó các tế bào và mô trải qua tái thiết22. Bởi vì KD không bắt buộc phải vào chế độ bỏ đói, không thúc đẩy sự phá vỡ lớn của các thành phần và mô nội bào và không bao gồm thời gian tái tạo, chúng không có khả năng gây ra kiểu tái sinh phối hợp được quan sát thấy trong quá trình nuôi LMLM.
Hạn chế calo
Trong khi chế độ hạn chế calo mãn tính (CR) và chế độ ăn uống thiếu các axit amin cụ thể rất khác so với chế độ ăn kiêng định kỳ, chúng có chung với nhịn ăn và bệnh FMD là hạn chế ít nhiều có chọn lọc các chất dinh dưỡng và chúng có tác dụng chống ung thư 81,89 112. CR thường liên quan đến việc giảm 20 30% năng lượng tiêu thụ mãn tính so với lượng calo tiêu chuẩn sẽ cho phép một cá nhân duy trì trọng lượng bình thường113,114. Nó rất hiệu quả trong việc giảm các yếu tố nguy cơ tim mạch và tỷ lệ mắc bệnh ung thư ở các sinh vật mô hình, bao gồm cả động vật linh trưởng108,109,114.
Tuy nhiên, CR có thể gây ra các tác dụng phụ, chẳng hạn như thay đổi ngoại hình, tăng nhạy cảm với lạnh, giảm sức mạnh, kinh nguyệt không đều, vô sinh, mất ham muốn tình dục, loãng xương, vết thương chậm lành hơn, ám ảnh thức ăn, cáu kỉnh và trầm cảm. Ở những bệnh nhân bị ung thư, có những lo ngại đáng kể rằng nó có thể làm trầm trọng thêm tình trạng suy dinh dưỡng và chắc chắn nó sẽ gây ra tình trạng mất quá nhiều khối lượng cơ thể nạc18,113 116. CR làm giảm lượng đường huyết lúc đói, mặc dù chúng vẫn ở trong giới hạn bình thường114. Ở người, CR mãn tính không ảnh hưởng đến mức IGF1 trừ khi thực hiện hạn chế protein vừa phải117.
Các nghiên cứu cho thấy bằng cách giảm tín hiệu mTORC1 trong các tế bào Paneth, CR làm tăng chức năng tế bào gốc của chúng và nó cũng bảo vệ các tế bào gốc ruột dự trữ khỏi tổn thương DNA 118,119, nhưng không biết liệu các tác dụng tái tạo ở các cơ quan khác cũng được CR gợi ra. Do đó, dữ liệu có sẵn cho thấy rằng nhịn ăn và FMD tạo ra một hồ sơ trao đổi chất, tái tạo và bảo vệ khác biệt và có thể mạnh hơn so với được gợi ra bởi một KD hoặc CR.
Nhịn ăn & FMD trong trị liệu: Ảnh hưởng đến mức độ hormone và chất chuyển hóa
Nhiều thay đổi về mức độ lưu thông của các hoocmon và các chất chuyển hóa thường thấy khi phản ứng với việc nhịn ăn có khả năng gây ra tác dụng chống độc (nghĩa là giảm mức glucose, IGF1, insulin và leptin và tăng mức adiponectin) 23,120,121 và / hoặc để đủ khả năng bảo vệ các mô khỏe mạnh khỏi các tác dụng phụ (nghĩa là giảm mức độ IGF1 và glucose). Do cơ thể ketone có thể ức chế histone deacetylase (HDACs), sự gia tăng nhanh chóng của cơ thể ketone có thể giúp làm chậm sự phát triển của khối u và thúc đẩy sự biệt hóa thông qua cơ chế biểu sinh122.
Tuy nhiên, acetoacetate trong cơ thể xeton đã được chứng minh là có tác dụng đẩy nhanh, thay vì làm giảm sự phát triển của một số khối u, chẳng hạn như u hắc tố có BRAF123 đột biến. Những thay đổi đó là bằng chứng mạnh mẽ nhất về vai trò trong tác dụng có lợi của việc nhịn ăn và bệnh FMD đối với bệnh ung thư là giảm mức IGF1 và glucose. Ở cấp độ phân tử, nhịn ăn hoặc FMD làm giảm các dòng tín hiệu nội bào bao gồm tín hiệu IGF1R AKT mTOR S6K và cAMP PKA, tăng khả năng tự động, giúp các tế bào bình thường chịu được căng thẳng và thúc đẩy khả năng miễn dịch chống ung thư25,29,56,124
Kháng stress khác biệt: Tăng khả năng dung nạp hóa trị
Một số chỉnh hình nấm men oncogene, chẳng hạn như Ras và Sch9 (chỉnh hình chức năng của động vật có vú S6K), có thể làm giảm sức đề kháng căng thẳng trong các sinh vật mô hình27,28. Ngoài ra, các đột biến kích hoạt IGF1R, RAS, PI3KCA hoặc AKT hoặc PTEN bất hoạt, có mặt trong phần lớn các bệnh ung thư ở người10. Cùng với nhau, điều này dẫn đến giả thuyết rằng việc bỏ đói sẽ gây ra tác dụng ngược trong ung thư so với các tế bào bình thường về khả năng chống lại các tác nhân gây căng thẳng tế bào, bao gồm cả hóa trị liệu. Nói cách khác, chết đói có thể dẫn đến
Theo giả thuyết DSR, các tế bào bình thường phản ứng với sự đói bằng cách điều chỉnh giảm sự tăng sinh liên quan và các gen lắp ráp và sinh học ribosome, buộc các tế bào phải đi vào chế độ tự duy trì và bảo vệ chúng khỏi những tổn thương do hóa trị, xạ trị và các tác nhân độc hại khác gây ra. Ngược lại, trong các tế bào ung thư, chế độ tự duy trì này bị ngăn chặn thông qua các thay đổi gây ung thư, gây ra sự ức chế cấu thành các con đường phản ứng với căng thẳng12 (Hình 1). Phù hợp với mô hình DSR, chết đói trong thời gian ngắn hoặc xóa bỏ proto-oncogene
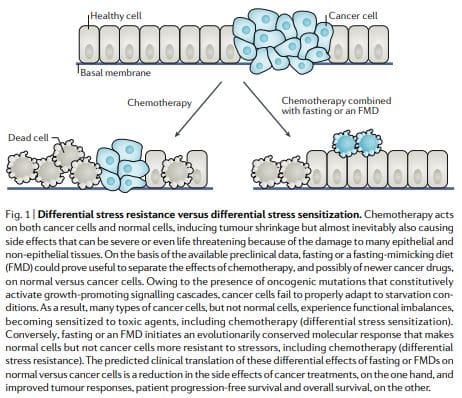
Các kết quả tương tự cũng thu được ở các tế bào động vật có vú: tiếp xúc với các tế bào glia nguyên phát của chuột có hàm lượng glucose thấp chống lại độc tính từ hydro peroxide hoặc cyclophosphamide (một hóa trị liệu prooxidant) nhưng không bảo vệ các dòng tế bào ung thư chuột, chuột và u nguyên bào thần kinh. Phù hợp với những quan sát này,
Các nghiên cứu tiếp theo phát hiện ra rằng việc giảm tín hiệu IGF1 trong phản ứng với nhịn ăn sẽ bảo vệ tế bào thần kinh đệm và tế bào thần kinh chính, nhưng không bảo vệ tế bào u thần kinh đệm và u nguyên bào thần kinh, khỏi cyclophosphamide và các hợp chất chống oxy hóa, đồng thời bảo vệ nguyên bào sợi phôi chuột khỏi doxorubicin29. Chuột thiếu IGF1 ở gan (LID), động vật chuyển gen có điều kiện xóa gen Igf1 ở gan có biểu hiện giảm 70-80% mức IGF1 lưu hành (mức tương tự như mức đạt được trong 72 giờ nhanh ở chuột) 29,125, đã được bảo vệ chống lại ba trong số bốn loại thuốc hóa trị được thử nghiệm, bao gồm cả doxorubicin.
Các nghiên cứu mô học cho thấy dấu hiệu của bệnh cơ tim do doxorubicin chỉ ở những con chuột đối chứng được điều trị bằng doxorubicin mà không phải ở những con chuột bị LID. Trong các thí nghiệm với động vật mang khối u ác tính được điều trị bằng doxorubicin, không quan sát thấy sự khác biệt về tiến triển của bệnh giữa chuột đối chứng và chuột LID, cho thấy rằng tế bào ung thư không được bảo vệ khỏi hóa trị do mức IGF1 giảm. Tuy nhiên, một lần nữa, những con chuột LID mang khối u lại thể hiện lợi thế sống sót đáng kể so với những con đối chứng nhờ khả năng chịu đựng độc tính doxorubicin29. Do đó, về tổng thể, những kết quả này đã khẳng định rằng điều hòa IGF1 là cơ chế chính mà nhịn ăn làm tăng khả năng dung nạp hóa trị.
Cả hai chất ức chế dexamethasone và mTOR đều được sử dụng rộng rãi trong điều trị ung thư, vì tác dụng của chúng là chống nôn và
Những can thiệp này làm giảm hoạt động PKA trong khi tăng hoạt động AMPK và do đó kích hoạt EGR1, cho thấy rằng tín hiệu cAMP PKA làm trung gian cho DSR gây ra khi đói thông qua EGR1 (tham khảo 26). EGR1 cũng thúc đẩy sự biểu hiện của các peptit bảo vệ tim mạch, chẳng hạn như peptit natri lợi tiểu nhĩ (ANP) và peptit lợi tiểu natri loại B (BNP) trong mô tim, góp phần vào việc đề kháng với doxorubicin. Hơn nữa, nhịn ăn và / hoặc FMD có thể bảo vệ chuột khỏi bệnh cơ tim do doxorubicin gây ra bằng cách thúc đẩy quá trình tự động, có thể thúc đẩy sức khỏe tế bào bằng cách giảm sản xuất oxy phản ứng (ROS) thông qua việc loại bỏ các ty thể bị rối loạn chức năng và bằng cách loại bỏ các tập hợp độc hại.
Ngoài việc giảm độc tính do hóa trị liệu gây ra trong tế bào và tăng khả năng sống sót của những con chuột được điều trị bằng hóa chất, chu kỳ nhịn ăn còn gây tái tạo tủy xương và ngăn chặn sự ức chế miễn dịch do cyclophosphamide gây ra theo cách liên quan đến PKA và IGF1. Do đó, các kết quả tiền lâm sàng thuyết phục cho thấy khả năng nhịn ăn và FMDs để tăng khả năng dung nạp hóa trị và tránh các tác dụng phụ lớn. Bởi vì dữ liệu lâm sàng ban đầu hỗ trợ thêm cho tiềm năng này, các nghiên cứu tiền lâm sàng này xây dựng cơ sở lý luận vững chắc để đánh giá bệnh LMLM trong các thử nghiệm lâm sàng ngẫu nhiên với TEAE làm điểm kết thúc chính.
Nhạy cảm căng thẳng khác biệt: Tăng cái chết của tế bào ung thư
Nếu được sử dụng một mình, hầu hết các can thiệp chế độ ăn uống, bao gồm nhịn ăn và FMD, có tác dụng hạn chế chống lại tiến triển ung thư. Theo giả thuyết nhạy cảm với căng thẳng khác biệt (DSS), sự kết hợp giữa nhịn ăn hoặc FMD với điều trị thứ hai có triển vọng hơn nhiều so với 11,12. Giả thuyết này dự đoán rằng, trong khi các tế bào ung thư có thể thích nghi với nồng độ oxy và dinh dưỡng hạn chế, nhiều loại tế bào ung thư không thể thực hiện các thay đổi sẽ cho phép tồn tại trong môi trường thiếu chất dinh dưỡng và độc hại được tạo ra bởi sự kết hợp giữa nhịn ăn và hóa trị , ví dụ. Thí nghiệm sớm trong ung thư vú, khối u ác tính
Chúng tôi xem xét một phản ứng không phù hợp như vậy của các tế bào ung thư đối với các điều kiện đã thay đổi, bao gồm việc giảm mức độ IGF1 và glucose gây ra bởi việc nhịn ăn hoặc FMD như một cơ chế chính làm cơ sở cho

Bằng cách giảm lượng glucose sẵn có và tăng axit béo? Oxy hóa, nhịn ăn hoặc FMD cũng có thể thúc đẩy quá trình chuyển đổi từ quá trình đường phân hiếu khí (hiệu ứng Warburg) sang quá trình phosphoryl hóa oxy hóa ty thể trong tế bào ung thư, điều này cần thiết để duy trì sự phát triển của tế bào ung thư trong môi trường nghèo dinh dưỡng nhất50 (Hình 2). Việc chuyển đổi này dẫn đến tăng sản xuất ROS11 do tăng hoạt động hô hấp của ty thể và cũng có thể liên quan đến việc giảm tiềm năng oxy hóa khử của tế bào do giảm tổng hợp glutathione từ quá trình đường phân và con đường pentose phosphate50. Tác động kết hợp của việc tăng ROS và giảm bảo vệ chống oxy hóa làm tăng stress oxy hóa trong tế bào ung thư và khuếch đại hoạt động của hóa trị liệu. Đáng chú ý, bởi vì hoạt tính glycolytic cao được chứng minh bằng cách sản xuất nhiều lactate có khả năng dự báo tính hung hăng và xu hướng di căn ở một số loại ung thư129, tác dụng chống Warburg của việc nhịn ăn hoặc FMD có khả năng đặc biệt hiệu quả đối với các bệnh ung thư di căn và tích cực.
Ngoài một sự thay đổi trong quá trình trao đổi chất, nhịn ăn hoặc FMD gợi ra những thay đổi khác có thể thúc đẩy DSS trong các tế bào ung thư tuyến tụy. Ăn chay làm tăng mức độ biểu hiện của
Cuối cùng, nhịn ăn có thể điều chỉnh lại thụ thể leptin và hạ lưu của nó
Đáng chú ý, có khả năng nhiều loại tế bào ung thư, bao gồm AML29, có thể kháng thuốc bằng cách phá vỡ các thay đổi chuyển hóa do nhịn ăn hoặc FMD, một khả năng còn tăng lên do sự không đồng nhất về chuyển hóa đặc trưng cho nhiều bệnh ung thư129. Vì vậy, mục tiêu chính trong tương lai gần sẽ là xác định các loại ung thư dễ mắc phải nhất trong các chế độ ăn kiêng này bằng các dấu ấn sinh học. Mặt khác, khi được kết hợp với các liệu pháp tiêu chuẩn, nhịn ăn hoặc FMD hiếm khi dẫn đến việc kháng thuốc ở các mô hình chuột ung thư và khả năng chống lại việc nhịn ăn kết hợp với hóa trị cũng không phổ biến trong các nghiên cứu trong ống nghiệm, nhấn mạnh tầm quan trọng của việc xác định các liệu pháp, khi kết hợp với FMDs, tạo ra tác dụng độc mạnh chống lại các tế bào ung thư với độc tính tối thiểu đối với các tế bào và mô bình thường 11,17,50,55 57,59,124.
Tăng cường miễn dịch chống ung thư bằng cách nhịn ăn hoặc FMD
Dữ liệu gần đây cho thấy rằng nhịn ăn hoặc FMDs, và ở mức độ lớn hơn khi kết hợp với hóa trị liệu, kích hoạt sự mở rộng của các tiền thân bạch huyết và thúc đẩy
Chế độ ăn uống chống ung thư trong mô hình chuột
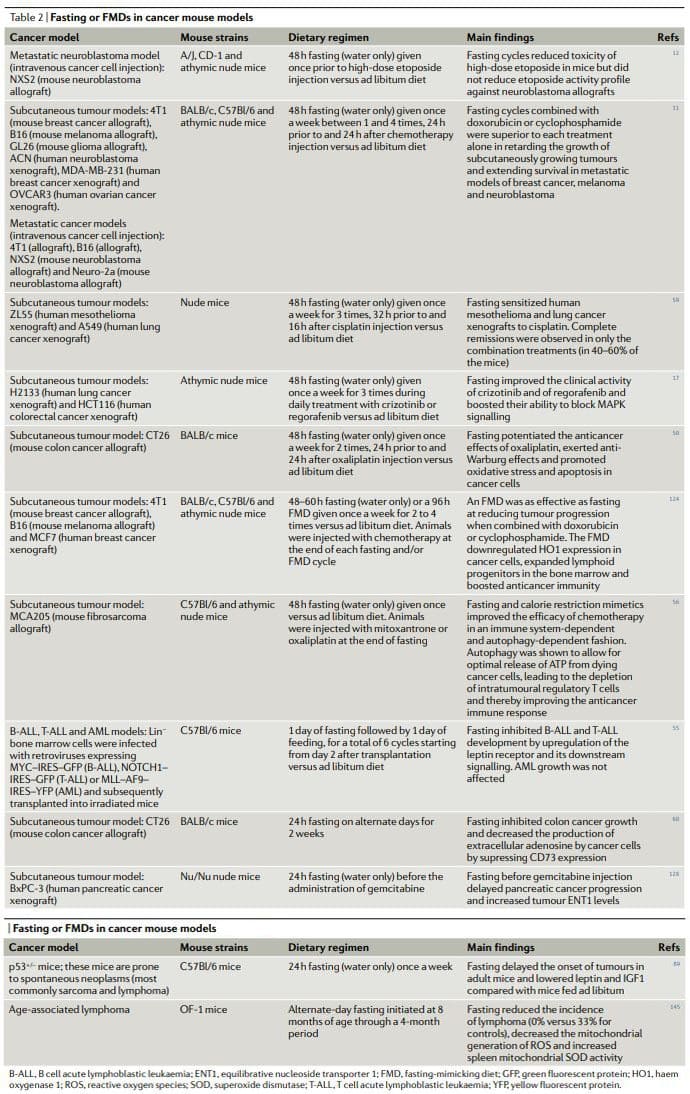
Nhìn chung, kết quả của các nghiên cứu tiền lâm sàng về nhịn ăn hoặc FMD trong các mô hình ung thư động vật, bao gồm các mô hình ung thư di căn (Bảng 2), cho thấy rằng nhịn ăn hoặc FMD định kỳ đạt được tác dụng chống ung thư toàn thân và tăng cường hoạt động của hóa trị liệu và TKI đồng thời có tác dụng bảo vệ và tái tạo ở nhiều cơ quan22,25. Để đạt được những hiệu quả tương tự mà không cần nhịn ăn và / hoặc FMD trước tiên cần xác định và sau đó là sử dụng nhiều loại thuốc hiệu quả, đắt tiền và thường xuyên độc hại và có thể sẽ không có lợi ích trong việc bảo vệ tế bào khỏe mạnh. Đáng chú ý là trong ít nhất hai nghiên cứu nhịn ăn kết hợp với hóa trị liệu được chứng minh là can thiệp duy nhất có khả năng đạt được sự thoái lui hoàn toàn của khối u hoặc sống sót lâu dài ở một phần nhỏ số động vật được điều trị11,59
KD mãn tính cũng cho thấy một
CR làm giảm sự hình thành khối u trong các mô hình ung thư chuột di truyền, mô hình chuột có khối u tự phát và mô hình chuột ung thư gây ra ung thư, cũng như ở khỉ 91,92,97,98,101,102,104 106,108,109,136 138. Ngược lại, một nghiên cứu cho thấy CR từ tuổi trung niên thực sự làm tăng tỷ lệ mắc ung thư tế bào huyết tương ở chuột C57Bl / 6. Tuy nhiên, trong cùng một nghiên cứu, CR cũng kéo dài tuổi thọ tối đa khoảng 139% và sự gia tăng tỷ lệ mắc bệnh ung thư được quan sát là do tuổi thọ của những con chuột trải qua CR tăng lên, ở độ tuổi mà
Quan trọng hơn, CR đã cải thiện hoạt động của điều trị chống ung thư trong một số mô hình ung thư, bao gồm hoạt động của một kháng thể chống ung thư (ganitumab) chống lại ung thư tuyến tiền liệt 1, cyclophosphamide chống lại các tế bào ung thư tuyến tiền liệt, ức chế tế bào ung thư tuyến tiền liệt trên tế bào ung thư tuyến tiền liệt Tuy nhiên, CR hoặc một KD kết hợp với các liệu pháp chống ung thư dường như ít hiệu quả hơn so với nhịn ăn. Một nghiên cứu trên chuột cho thấy, trái ngược với việc nhịn ăn một mình, CR không thể làm giảm sự phát triển của u thần kinh đệm GL141 dưới da và một lần nữa, ngược lại với việc nhịn ăn ngắn hạn, CR không làm tăng hoạt động của cisplatin đối với vú 135T12 dưới da tumours100. Trong cùng một nghiên cứu, nhịn ăn cũng tỏ ra hiệu quả hơn đáng kể so với CR và một KD trong việc tăng khả năng dung nạp của doxorubicin26. Mặc dù nhịn ăn hoặc FMD, CR và KD có thể hành động và điều chỉnh chồng chéo
Giai đoạn làm lại có thể sau đó
Ăn chay và FMD trong phòng chống ung thư
Các nghiên cứu và dịch tễ học ở động vật, bao gồm cả khỉ108,109,144 và con người cho vay hỗ trợ cho quan niệm rằng CR mãn tính và nhịn ăn định kỳ và / hoặc FMD có thể có tác dụng ngăn ngừa ung thư ở người. Tuy nhiên, CR khó có thể được thực hiện trong dân số nói chung do các vấn đề tuân thủ và các tác dụng phụ có thể xảy ra115. Do đó, trong khi các khuyến nghị dựa trên bằng chứng về thực phẩm nên (hoặc tránh) cũng như các khuyến nghị về lối sống để giảm nguy cơ ung thư đang được thiết lập, thì mục tiêu bây giờ là xác định và, có thể, tiêu chuẩn hóa chế độ ăn kiêng định kỳ, dung nạp tốt với mức độ thấp hoặc không tác dụng phụ và đánh giá hiệu quả phòng ngừa ung thư của họ trong các nghiên cứu lâm sàng.
Như đã thảo luận trước đó, các chu kỳ FMD gây ra sự điều hòa giảm của IGF1 và glucose và điều hòa lại các cơ thể IGFBP1 và ketone, những thay đổi tương tự như gây ra bởi việc nhịn ăn và là dấu ấn sinh học của phản ứng nhịn ăn 22. Khi chuột C57Bl / 6 (tự phát triển
Một nghiên cứu trước đây về việc nhịn ăn xen kẽ, được thực hiện ở những con chuột trung niên trong tổng số tháng 4, cũng cho thấy việc nhịn ăn làm giảm tỷ lệ mắc ung thư hạch, đưa nó từ 33% (đối với chuột đối chứng) thành 0% (nhịn ăn động vật) 145, mặc dù vì thời gian nghiên cứu ngắn nhưng không biết liệu chế độ nhịn ăn này có ngăn chặn được hay đơn giản là trì hoãn
Do đó, kết quả đầy hứa hẹn của các nghiên cứu tiền lâm sàng kết hợp với dữ liệu lâm sàng về tác động của FMD đối với các yếu tố nguy cơ đối với
Khả năng ứng dụng lâm sàng trong Ung bướu
Bốn nghiên cứu khả thi về nhịn ăn và FMD ở bệnh nhân trải qua hóa trị liệu đã được công bố tính đến ngày hôm nay52,53,58,61. Trong một loạt trường hợp bệnh nhân 10 được chẩn đoán mắc các loại ung thư khác nhau, bao gồm ung thư vú, tuyến tiền liệt, buồng trứng, tử cung, phổi và thực quản, những người đã tự nguyện nhịn ăn với 140hours trước và / hoặc lên đến 56hours sau khi hóa trị, không gây ra tác dụng phụ nào bằng cách nhịn ăn khác với đói và chóng mặt đã được báo cáo58. Những bệnh nhân (sáu) đã trải qua hóa trị liệu có và không nhịn ăn đã báo cáo giảm đáng kể tình trạng mệt mỏi, yếu và các tác dụng phụ đường tiêu hóa trong khi nhịn ăn. Ngoài ra, ở những bệnh nhân có thể đánh giá tiến triển ung thư, nhịn ăn không ngăn ngừa được việc giảm hóa trị do khối lượng khối u hoặc trong các dấu hiệu khối u. Trong một nghiên cứu khác, phụ nữ 13 với HER2 (còn được gọi là ERBB2) âm tính, ung thư vú giai đoạn II / III được điều trị bằng hóa chất tân dược taxotere, adriamycin và cyclophosphamide (TAC) đã được chọn ngẫu nhiên hóa nhanh (chỉ nước) trước khi bắt đầu hóa trị dinh dưỡng theo hướng dẫn tiêu chuẩn24.
Nhịn ăn ngắn hạn được dung nạp tốt và giảm lượng hồng cầu trung bình và số lượng tiểu cầu trong 7 ngày sau khi hóa trị. Điều thú vị là trong nghiên cứu này, mức độ? -H2AX (một dấu hiệu của tổn thương DNA) đã tăng lên 30 phút sau khi hóa trị trong bạch cầu từ những bệnh nhân không nhịn ăn nhưng không phải ở những bệnh nhân đã nhịn ăn. Trong một liều tăng dần khi nhịn ăn ở bệnh nhân đang hóa trị liệu dựa trên bạch kim, 20 bệnh nhân (được điều trị chủ yếu cho ung thư biểu mô, buồng trứng hoặc ung thư vú) được ngẫu nhiên nhịn ăn trong 24, 48 hoặc 72 giờ (chia làm 48 giờ trước khi hóa trị và 24 giờ sau khi hóa trị) ) 53. Tiêu chí khả thi (được định nghĩa là ba hoặc nhiều hơn trong số sáu đối tượng trong mỗi nhóm thuần tập tiêu thụ? 200kcal mỗi ngày trong thời gian nhanh mà không có độc tính dư thừa) đã được đáp ứng. Độc tính liên quan đến nhịn ăn
Gần đây, một thử nghiệm lâm sàng chéo ngẫu nhiên đã được tiến hành đánh giá ảnh hưởng của FMD đến chất lượng cuộc sống và tác dụng phụ của hóa trị liệu trong tổng số bệnh nhân 34 bị ung thư vú hoặc ung thư buồng trứng61. FMD bao gồm
Những thách thức trong phòng khám
Nghiên cứu về nhịn ăn định kỳ hoặc FMDs trong ung thư không phải là vấn đề đáng lo ngại, đặc biệt liên quan đến khả năng chế độ ăn kiêng này có thể làm giảm suy dinh dưỡng, sarcop giảm,
Kết luận
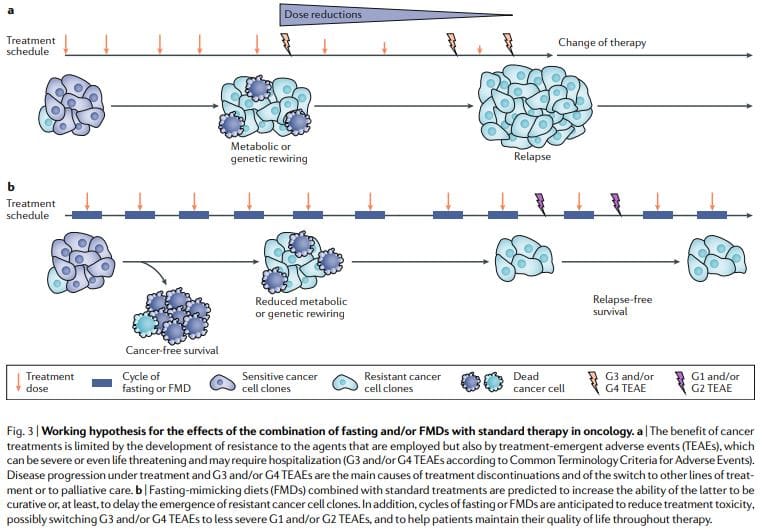
Nhịn ăn định kỳ hoặc FMD thường xuyên cho thấy tác dụng chống ung thư mạnh mẽ trong các mô hình ung thư ở chuột, bao gồm khả năng tăng cường hóa trị liệu và TKI và kích hoạt miễn dịch chống ung thư. LMLM chu kỳ khả thi hơn so với chế độ ăn kiêng mãn tính vì chúng cho phép bệnh nhân tiêu thụ thức ăn thường xuyên trong thời gian mắc bệnh LMLM, duy trì chế độ ăn bình thường giữa các chu kỳ và không dẫn đến sụt cân nghiêm trọng và có thể ảnh hưởng bất lợi đến hệ thống miễn dịch và nội tiết. Đáng chú ý, vì các liệu pháp độc lập, chu kỳ nhịn ăn hoặc FMD định kỳ có thể cho thấy hiệu quả hạn chế đối với các khối u đã hình thành. Trên thực tế, ở chuột, nhịn ăn hoặc FMD ảnh hưởng đến sự tiến triển của một số bệnh ung thư tương tự như hóa trị, nhưng riêng lẻ, chúng hiếm khi phù hợp với hiệu quả thu được khi kết hợp với thuốc điều trị ung thư có thể dẫn đến sự sống sót không bị ung thư11,59. Do đó, chúng tôi đề xuất rằng sự kết hợp của các chu kỳ FMD định kỳ với các phương pháp điều trị tiêu chuẩn có tiềm năng cao nhất để thúc đẩy sự sống sót không bị ung thư ở bệnh nhân, như được đề xuất bởi các mô hình chuột11,59 (Hình 3).
Sự kết hợp này có thể đặc biệt mạnh vì nhiều lý do: đầu tiên, thuốc trị ung thư và các phương pháp điều trị khác có thể có hiệu quả, nhưng một phần bệnh nhân không đáp ứng vì các tế bào ung thư áp dụng các chiến lược chuyển hóa thay thế dẫn đến sự sống còn. Các chế độ trao đổi chất thay thế này khó khăn hơn nhiều để duy trì trong điều kiện nhịn ăn hoặc FMD do thiếu hụt hoặc thay đổi glucose, một số axit amin, hormone và các yếu tố tăng trưởng, cũng như trong các con đường chưa biết khác dẫn đến chết tế bào. Thứ hai, nhịn ăn hoặc FMD có thể ngăn ngừa hoặc làm giảm sự kháng thuốc. Thứ ba, nhịn ăn hoặc FMD bảo vệ các tế bào và cơ quan bình thường khỏi các tác dụng phụ gây ra bởi nhiều loại thuốc ung thư. Trên cơ sở bằng chứng lâm sàng và tiền lâm sàng về tính khả thi, an toàn và hiệu quả (tại việc giảm IGF1, mỡ nội tạng
Hơn nữa, điều cần thiết là áp dụng FMD với sự hiểu biết về các cơ chế hoạt động, vì tiềm năng của chúng
Các nghiên cứu lâm sàng đang diễn ra về bệnh LMLM ở bệnh nhân ung thư 63,65-68 sẽ cung cấp câu trả lời chắc chắn hơn về việc liệu kê đơn định kỳ FMD kết hợp với các thuốc chống ung thư thông thường có giúp cải thiện khả năng dung nạp và hoạt động của bệnh sau này hay không. Điều quan trọng cần lưu ý là FMDs sẽ không hiệu quả trong việc giảm tác dụng phụ của phương pháp điều trị ung thư ở tất cả bệnh nhân và chúng cũng không có tác dụng cải thiện hiệu quả của tất cả các liệu pháp, nhưng chúng có tiềm năng rất lớn để làm như vậy ít nhất là đối với một phần và có thể cho một bộ phận chính bệnh nhân và thuốc. Những bệnh nhân ốm yếu hoặc suy dinh dưỡng hoặc những bệnh nhân có nguy cơ suy dinh dưỡng không nên tham gia vào các nghiên cứu lâm sàng về nhịn ăn hoặc bệnh LMLM, và tình trạng dinh dưỡng của bệnh nhân và chứng chán ăn phải được theo dõi cẩn thận trong suốt các thử nghiệm lâm sàng.
Tài liệu tham khảo:
Phạm vi hành nghề chuyên nghiệp *
Thông tin ở đây về "Ăn chay và ung thư: Cơ chế phân tử và ứng dụng lâm sàng" không nhằm mục đích thay thế mối quan hệ trực tiếp với chuyên gia chăm sóc sức khỏe đủ điều kiện hoặc bác sĩ được cấp phép và không phải là lời khuyên y tế. Chúng tôi khuyến khích bạn đưa ra quyết định chăm sóc sức khỏe dựa trên nghiên cứu và quan hệ đối tác của bạn với chuyên gia chăm sóc sức khỏe đủ điều kiện.
Thông tin Blog & Thảo luận Phạm vi
Phạm vi thông tin của chúng tôi được giới hạn trong Trị liệu thần kinh cột sống, cơ xương khớp, thuốc vật lý, sức khỏe, góp phần gây bệnh rối loạn nội tạng trong các bài thuyết trình lâm sàng, động lực học phản xạ somatovisceral liên quan đến lâm sàng, các phức hợp hạ lưu, các vấn đề sức khỏe nhạy cảm và / hoặc các bài báo, chủ đề và thảo luận về y học chức năng.
Chúng tôi cung cấp và trình bày cộng tác lâm sàng với các chuyên gia từ nhiều lĩnh vực khác nhau. Mỗi chuyên gia được điều chỉnh bởi phạm vi hành nghề chuyên nghiệp và thẩm quyền cấp phép của họ. Chúng tôi sử dụng các phác đồ chăm sóc sức khỏe & sức khỏe chức năng để điều trị và hỗ trợ chăm sóc các chấn thương hoặc rối loạn của hệ thống cơ xương.
Các video, bài đăng, chủ đề, chủ đề và thông tin chi tiết của chúng tôi đề cập đến các vấn đề, vấn đề và chủ đề lâm sàng liên quan và trực tiếp hoặc gián tiếp hỗ trợ phạm vi hành nghề lâm sàng của chúng tôi.*
Văn phòng của chúng tôi đã cố gắng một cách hợp lý để cung cấp các trích dẫn hỗ trợ và đã xác định nghiên cứu nghiên cứu có liên quan hoặc các nghiên cứu hỗ trợ bài đăng của chúng tôi. Chúng tôi cung cấp các bản sao của các nghiên cứu hỗ trợ có sẵn cho các hội đồng quản lý và công chúng theo yêu cầu.
Chúng tôi hiểu rằng chúng tôi bao gồm các vấn đề cần giải thích thêm về cách nó có thể hỗ trợ trong một kế hoạch chăm sóc hoặc phác đồ điều trị cụ thể; do đó, để thảo luận thêm về vấn đề trên, vui lòng hỏi Tiến sĩ Alex Jimenez, DC, hoặc liên hệ với chúng tôi tại 915-850-0900.
Chúng tôi ở đây để giúp bạn và gia đình bạn.
Blessings
Tiến sĩ Alex Jimenez A.D, MSACP, RN*, CCST, IFMCP*, CIFM*, ATN*
email: coach@elpasofeftalmedicine.com
Được cấp phép là Bác sĩ Chiropractic (DC) tại Texas & New Mexico*
Giấy phép Texas DC # TX5807, Giấy phép New Mexico DC # NM-DC2182
Được cấp phép làm Y tá đã Đăng ký (RN*) in Florida
Giấy phép Florida Giấy phép RN # RN9617241 (Số kiểm soát 3558029)
Trạng thái nhỏ gọn: Giấy phép đa bang: Được phép hành nghề tại Hoa Kỳ*
Tiến sĩ Alex Jimenez DC, MSACP, RN* CIFM*, IFMCP*, ATN*, CCST
Danh thiếp kỹ thuật số của tôi